У человека количество постоянных зубов строго ограничено 32. Однако это число может уменьшаться генетически (это происходит у 1% населения) в рамках явления, известного как врожденная анодонтия. Анодонтия характеризуется отсутствием всех зубов, а отсутствие более 6 зубов называется «олигодонтия». Эти состояния, известные как «зубной агенезис», проявляются с раннего возраста и препятствуют способности правильно есть и говорить.
С другой стороны, 1% населения Земли имеет противоположное врожденное состояние: гипердонтия — состояние, при котором количество зубов превышает норму. По мнению исследователей из Университета Киото и Фукуи, это явление связано с ростом третьего ряда зубов, способности, которую большинство из нас утратило в ходе эволюции.
Некоторые животные, например, акулы и некоторые виды рептилий и грызунов, могут отращивать свои зубы бесконечно на протяжении всей жизни. И хотя считалось, что у человека существует только два набора зубов, недавно исследователи обнаружили «спящие почки» третьего поднабора. Стимуляция этих почек могла бы в большей или меньшей степени обеспечить такую же способность к регенерации зубов, которая наблюдается у вышеупомянутых животных.
«Идея выращивания новых зубов — мечта любого стоматолога«, — говорит Кацу Такахаши, ведущий исследователь и заведующий отделением стоматологии и челюстно-лицевой хирургии в больнице Китано (Осака). В своем исследовании, опубликованном в журнале Science Advances, Такахаши и его коллеги выявили многообещающий генетический путь, конкретно участвующий в управлении развитием зубов и ростом третьего подмножества зубов.
Это открытие позволило им разработать моноклональное антитело, нацеленное на соответствующий ген. Хотя изначально молекула предназначена для детей в возрасте от 2 до 6 лет, страдающих от врожденного анодонтизма, она также может быть использована для лечения патологической (прогрессирующий кариес, эрозия зубных альвеол и т.д.) или травматической потери зубов. «В любом случае, мы надеемся, что настанет время, когда препараты для восстановления зубов станут третьим выбором наряду с протезами и имплантатами«, — объясняет Такахаши.
Препарат на основе моноклональных антител
Рост отдельных зубов зависит от взаимодействия нескольких молекул, в частности BMP (костный морфогенный протеин) и сигнального пути Wnt. Предыдущие исследования показали, что BMP способствует образованию дополнительных зубов, а Wnt вызывает образование сверхкомплектных зубов при таких заболеваниях, как гипердонтия.
Однако участие обоих сигнальных путей в строгом определении количества зубов (32 в нашем случае) остается неясным. Кроме того, они вовлечены во многие другие биологические процессы, помимо роста зубов, такие как развитие скелета. Некоторые из этих процессов модулируются с эмбриональной стадии. В результате их активация напрямую сопряжена со значительными рисками.
Чтобы компенсировать эти потенциальные риски, японские исследователи выбрали USAG-1, бифункциональный белок, который антагонизирует пути BMP и Wnt. Поскольку этот белок является антагонистом и подавляет рост зуба, его деактивация с помощью антитела может возобновить этот рост. «Обычная тканевая инженерия не подходит для регенерации зубов. Наше исследование показывает, что ацеллюлярная молекулярная терапия эффективна для широкого спектра врожденных зубных агенезий«, — говорит Манабу Сугаи из Университета Фукуи, соавтор исследования.
Чтобы подтвердить свою гипотезу, исследователи протестировали на мышах ряд моноклональных антител против UСАG-1. Некоторые из них вызывали низкую рождаемость и выживаемость, что подтверждает важную роль BMP и Wnt в эмбриональном развитии. В отличие от них, антитело, блокирующее только взаимодействие USAG-1 с BMP, оказалось более успешным. В экспериментах одного введения антитела было достаточно для формирования зуба третьего поколения. Эксперты также обнаружили, что передача сигналов играет важную роль в определении количества зубов у мышей.
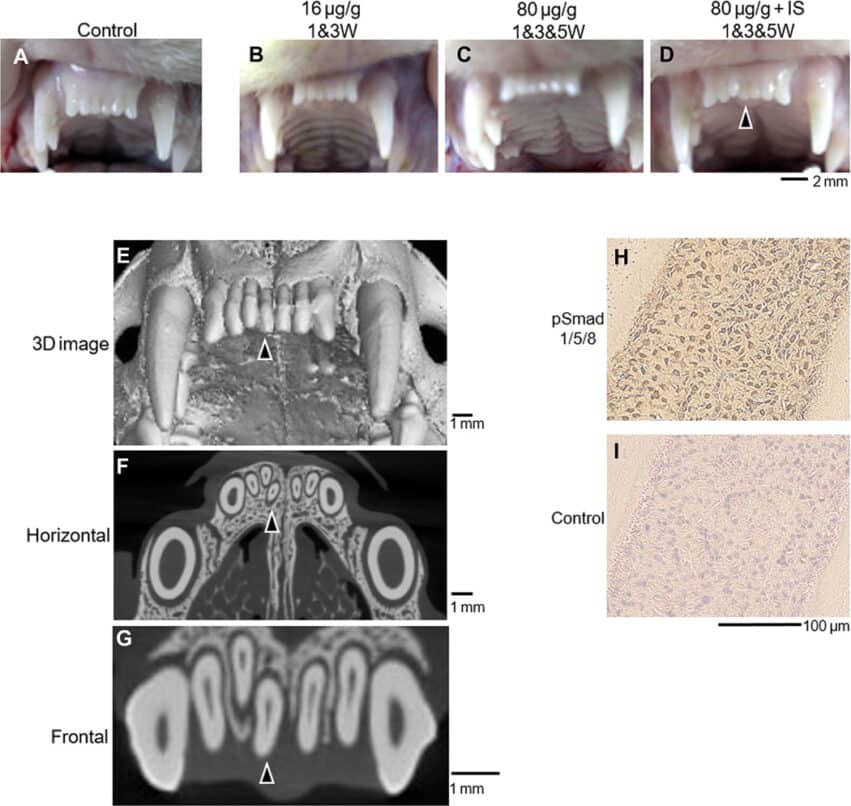
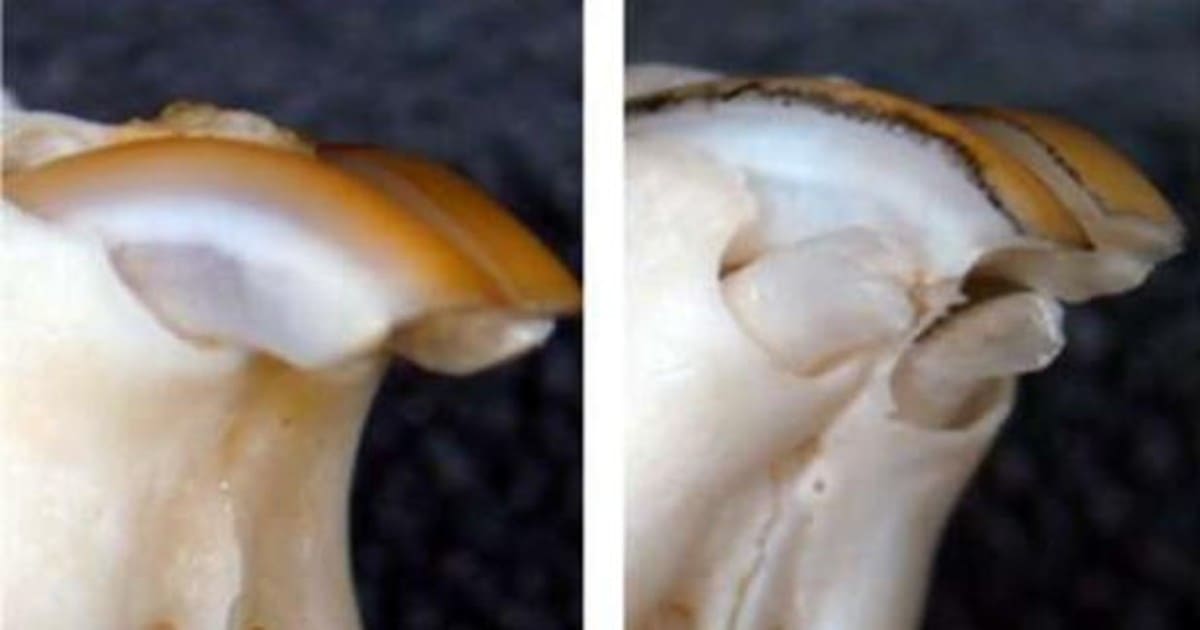
При повторении эксперимента на хорьках вырос дополнительный седьмой зуб. Учитывая, что зуб вырос между существующими и имел такую же форму, исследователи пришли к выводу, что это зуб третьего поколения. В ближайшем будущем безопасность и эффективность антитела будут проверены in vivo на других животных. Затем препарат может вступить в фазу клинических испытаний уже в июле 2024 года.
