C. albicans, наряду с другими видами рода Candida, является естественной частью комменсальной микробиоты наших слизистых оболочек. Однако становясь условно-патогенной (например, при иммунодефиците), он иногда может вызывать серьезные инфекции. Церебральный микоз, вызываемый этим видом, является наиболее распространенной формой церебрита. Эти грибки были также обнаружены в мозге людей, страдающих болезнью Альцгеймера и другими хроническими нейродегенеративными заболеваниями. Удивительно, но у этих пациентов не наблюдалось ни симптомов острой инфекции, таких как лихорадка, ни быстрого ухудшения психического состояния. Это означает, что микробная инфекция мозга не вызывает «стерилизующего» иммунитета и в некоторых случаях может сохраняться в течение длительного времени.
В последнее время в некоторых исследованиях высказывается предположение о микробном происхождении болезни Альцгеймера. В 2019 году ученые продемонстрировали, что, проникая в мозг, представители рода Candida вызывают изменения, сходные с теми, которые наблюдаются при этом заболевании.
Новое исследование, опубликованное в журнале и проведенное под руководством той же группы экспертов, что и исследование 2019 года, было направлено на дальнейшее изучение биомолекулярных механизмов, лежащих в основе этой связи, уделяя особое внимание C. albicans, ответственному за половину случаев кандидоза. Несмотря на растущее количество доказательств участия грибка в патологии, точный способ его влияния до конца не изучен. «Эта работа может стать новой важной частью головоломки в развитии болезни Альцгеймера«, — говорит автор исследования Дэвид Корри из Медицинского колледжа Бэйлора.
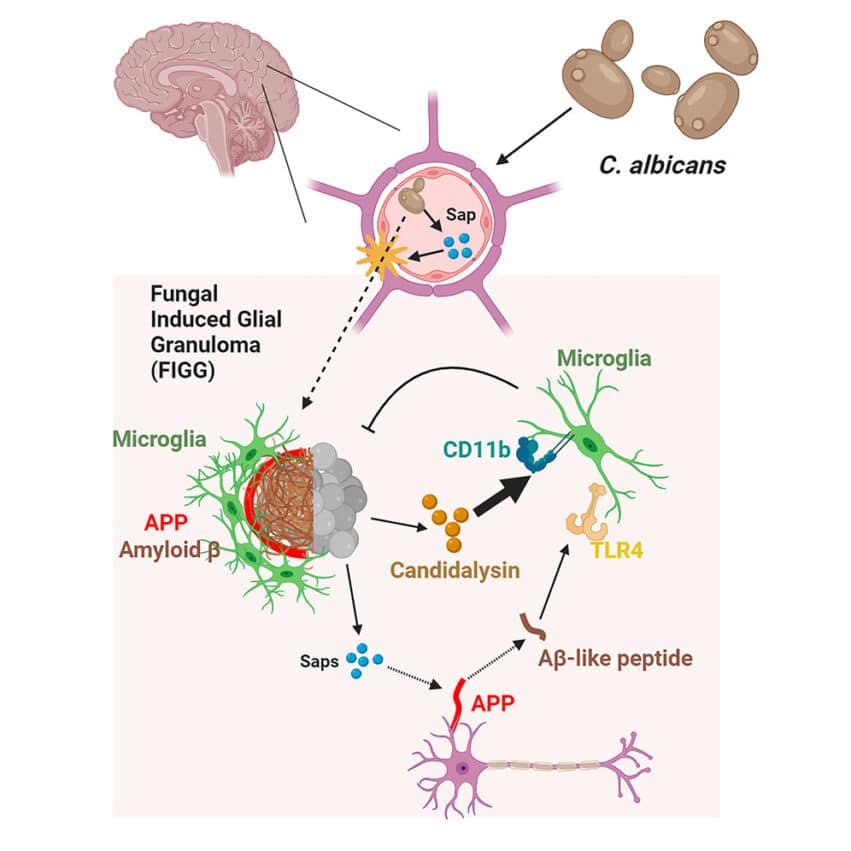
Два процесса, связанных с накоплением β-амилоидных пептидов
Когда грибки попадают в организм или становятся условно-патогенными, они обычно вызывают фагоцитарный, пептидный, окислительный и воспалительный иммунный ответ. C. albicans специфически распознается иммунной системой благодаря выделяемому им пептидному токсину кандидализину. Удивительно, но во время острого церебрального микоза низкой степени тяжести, вызванного этими грибами, макрофаги, нейтрофилы и лимфоциты, которые должны активироваться, не обнаруживаются в мозге мышиных моделей. Вместо этого происходит сильная активация микроглии, приводящая к разрушению мозга. Исследователи из Медицинского колледжа Бэйлора ранее показали, что у мышей, не имеющих основного заболевания, грибковая инфекция полностью уничтожается через 10 дней.
Однако процесс, приводящий к клиренсу (соотношение между количеством вещества, выведенного за единицу времени, и концентрацией того же вещества в жидкости организма) грибка, остается малоизученным, как и то, каким образом ему удается преодолеть гематоэнцефалический барьер. Способность C. albicans быстро проникать в мозг системным путем позволяет предположить, что он использует особый механизм для нарушения структуры этого барьера. Учитывая, что целостность этого барьера частично основана на плотных белковых соединениях, авторы исследования предположили, что для его преодоления дрожжи запускают протеолиз. Грибок выделяют 10 аспаргиновых протеиназ (Saps), которые достаточно мощны, чтобы разрушить большинство человеческих белков.
Исследователи подтвердили эту гипотезу, проведя повторную работу на мышиных моделях. Кроме того, они отметили, что, попадая в паренхиму мозга, Saps также разрушают белок-предшественник амилоида (APP), экспрессирующийся в нейронах в виде β-амилоидных пептидов и связывающийся с микроглиальным активатором Toll-like receptor 4 (TLR4). Этот механизм направлен на уничтожение грибов в мозге (клиренс), что позволяет поддерживать низкую грибковую нагрузку, но не устраняет их полностью.
С другой стороны, кандидализин, продуцируемый грибом, также способствует его выведению путем связывания с микроглией через рецептор интегрина CD11b. Нарушение этого пути приводит к длительной инфекции. «Опосредованная кандидализином активация микроглии необходима для элиминации C. albicans в мозге. Если мы удалим этот путь, грибки больше не будут эффективно вымываться из мозга«, — говорит ведущий автор исследования Ифань Ву из Медицинского колледжа Бэйлора.
В целом, изменение этих процессов клиренса приводит к токсическому накоплению β-амилоидных пептидов, что может привести к нейродегенерации. Важно отметить, что обычно считается, что собственные протеазы мозга могут приводить к эндогенному накоплению этих пептидов. В настоящем исследовании показано, что эти пептиды могут генерироваться из другого источника. «Мы предполагаем, что мозговые агрегаты β-амилоидных пептидов, характерные для ряда нейродегенеративных заболеваний, вызванных Candida (болезнь Альцгеймера, болезнь Паркинсона и т.д.), могут генерироваться как мозгом, так и грибком«, — предполагает Корри. Эти результаты потенциально могут привести к разработке более эффективных терапевтических стратегий.
