Испытание терапевтических подходов к нейродегенеративным заболеваниям может проводиться на генно-модифицированных мышах или культуре человеческих клеток. В первом случае успешность эксперимента не гарантирует безопасности и эффективности препарата для человека. Во втором требуется длительное время для развития нейронов до состояния, сходного с возрастом клеток мозга пациентов с нейродегенеративными заболеваниями. Новая модельная клеточная культура, разработанная в США, решает эту проблему.
Большинство нейродегенеративных болезней обусловлены сбоями функционирования тау-белка. MAPTТау-белки являются ключевым элементом цитоскелета нейронов. Такие заболевания называются таупатиями. К ним относятся болезни Альцгеймера и Пика, прогрессирующий надъядерный парез взора, кортикобазальная дегенерация.
С возрастом в клетках часто наблюдается избыточное фосфорилирование тау-белка и его модификаций. MAPTНе микротрубочки цитоскелета формирует, а нейрофибриллярные клубки. Эти структуры постепенно нарушают нормальную жизнедеятельность нейронов и наряду с прочими патологическими изменениями, зависящими от конкретного заболевания, приводят к системной утрате функций нервной системы.
Процессы эти изучать затруднительно из-за их медленного развития. В моделях организмов и культурах клеток человека формирование признаков нейродегенеративных заболеваний занимает много месяцев. С мышами такой срок еще приемлем: исследователи привыкли содержать выводки подопытных животных в разной степени готовности к экспериментам. Это недешево и хлопотно, а результаты не всегда применимы к людям. Тем не менее технология отработана и обладает хорошей результативностью.
Выращивание, контроль и поддержание клеточной культуры в строго заданных условиях продолжительное время — задача значительной сложности, особенно если речь идет о дорогих культурах человеческих стволовых клеток. Однако результаты с точки зрения медицины куда ценнее. В общем, идеального решения не существует, все варианты проблематичны.
Существует ещё одно ограничение: человеческие плюрипотентные стволовые клетки . hiPSCНейроны, специализирующиеся на этом, вырабатывают очень мало. 4RИзоформ тау-белка важна для изучения патологических процессов, связанных с нейродегенеративными заболеваниями. Для поиска действенных методов сдерживания таупатий необходимо культивировать клетки не месяцы, а годы или даже десятилетия. 4RВ нейронах изоформы просто не смогут скапливаться. Такой метод чрезмерно труден и затратен.
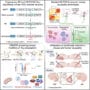
Новая клеточная культура с мутацией сможет оказать поддержку. P301SВ гене, отвечающем за выработку тау-белка, изменены плюрипотентные стволовые клетки человека, направленные на специализацию в нейроны. Последний тип клеток производит увеличенное количество MAPTСпособны накопить необходимые объёмы различных изоформ данного белка. 4R, за считанные недели.
Для повышения качества результатов американские учёные применяют… CRISPRПроведя интерференцию (селективное «выключение» генов), исследователи проанализировали тысячу генов и оценили их влияние на производство тау-белка. В результате удалось выделить 500 генов, участвующих в этом процессе.
Одним из перспективных открытий, представленных в данной научной публикации, является роль белка. UFM1Изучается белок, а точнее — цепочка реакций, происходящих при его контакте с другими молекулами в нервных клетках. Раньше в головном мозге умерших больных болезнью Альцгеймера выявлялись сбои в функционировании UFM1Хотя процесс был известен, детально его никто не изучал. Теперь учёные наглядно продемонстрировали: для ограничения распространения тау-белков в клетке достаточно остановить работу фермента, важного для их действия. UFM1-каскада.
В Медицинском колледже Вейля Корнеллского университета создали новую клеточную культуру. Weill Cornell MedicineПри участии коллег из ведущих научно-исследовательских и медицинских учреждений США и Канады проведена научная работа. В работе описана методика создания новой клеточной культуры человеческих нейронов и результаты экспериментов по тестированию целей для терапии нейродегенеративных заболеваний. опубликована в рецензируемом журнале Cell.