Подавление метаболизма глутамина истощает клетки опухолей и улучшает иммунный ответ.

Ученые из Центра медицинских исследований имени Джонса Хопкинса разработали соединение, которое способно замедлить рост опухоли, изменить ее микроокружение и способствовать появлению высокоактивных противоопухолевых лимфоцитов. Статья об этом опубликована в журнале Science.
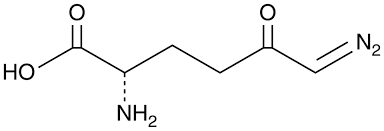
Новое вещество под кодовым обозначением JHU083 — пролекарственная форма (вещество, которое трансформируется в лекарство уже в организме) 6-диазо-5-оксо-L-норлейцина (DON), нестандартной аминокислоты, выделенной из бактерий рода Streptomyces. Благодаря определенному структурному сходству с глутамином, DON способен нарушать его метаболизм, блокируя активные центры ферментов.
Глутамин играет важную роль в опухолевом метаболизме. Эта аминокислота присутствует во всех тканях организма и является предшественником АТФ — главного источника энергии для биохимических процессов. Раковые клетки интенсивно делятся и могут при этом использовать глутамин в качестве основного «топлива» для роста. Поэтому блокирование окисления глутамина может помочь в борьбе с раком.
Хотя глутамин способны утилизировать любые клетки, пролекарство DON нацелено именно на клетки опухолей, ведь они, по словам ученых, «наиболее голодны». Но преимущество нового препарата не только в его избирательном действии: метаболическая терапия при помощи DON имеет определенный иммунотерапевтический эффект, положительно влияя на противоопухолевые свойства Т-лимфоцитов.
Ученые протестировали JHU083 на мышах с меланомой, лимфомой и раком толстой кишки. Применение этого вещества снижало рост опухоли и повышало выживаемость мышей на различных стадиях заболевания, а некоторых грызунов даже удалось вылечить полностью. Но самым интересным было то, что при повторном введении опухолевых клеток организм выздоровевших мышей отторгал их. Исследователи предположили, что под влиянием JHU083 у животных сформировалась иммунная память, благодаря которой лимфоциты сразу распознавали мутировавшие клетки.
Оказалось, раковые клетки и клетки иммунной системы по-разному реагировали на глутаминовую блокаду. Применение JHU083 приводило к истощению опухолей и клеток в их микроокружении, но делало Т-лимфоциты более активными. «Блокируя метаболизм глутамина, мы делали эти клетки более устойчивыми, больше похожими на клетки иммунной памяти», — говорит ведущий автор исследования Джонатан Пауэлл.
Ученые также установили, что применение пролекарства повышает эффективность адоптивной иммунотерапии — метода лечения, при котором пациентам вводят специально выращенные в лаборатории T-лимфоциты для усиления иммунного ответа. В последующих исследованиях Пауэлл и его коллеги хотят изучить, как JHU083 сочетается с различными видами иммунотерапии, и выяснить, могут ли определенные опухоли преодолевать «метаболическую ловушку», созданную новым препаратом.
