В результате экспериментов с пептидами американские химики предложили новое объяснение гомохиральности молекул, из которых формируется жизнь. Пояснениям служит дисбаланс односторонних молекул в начальном составе.
Большинство биологических молекул хирально, то есть имеют зеркальное отражение, как правая и левая ладони. энантиомеровСтереоизомеры — это формы, идентичные по строению, но не совпадающие в пространстве. Однако молекулы, из которых строится жизнь, по неизвестной причине лишены хиральных дубликатов. Такая особенность называется гомохиральностью или хиральной чистотой. В обычных химических реакциях две смеси с лево- и правосторонними молекулами ( рацемические смесиВ целом похожи, но в биологических — наоборот. Смесь из молекул с измененной структурой будет инертной или даже токсичной, то есть не станет живой.
Учёные давно стремятся разобраться, почему молекулы жизни — аминокислоты, углеводы, пептиды — практически всегда обнаруживаются только в одной форме. Структуры ДНК и РНК, а также белки создаются из молекул, у которых нет пары стереоизомеров: только левовращательные L-аминокислоты и правовращательные D-нуклеотиды. Само ДНК закручено только влево. ПредполагалиВысказывалось предположение, что гомохиральность определяется различием физических свойств молекул. версияВсё из-за случая, когда синтез исходных веществ для молекул был нарушен.
Новое исследование, опубликованное в журнале NatureИсследователи из американского центра The Scripps Research Institute приносят новое понимание этой загадки, синтезировав комплекты пептидов и изучив принципы хирального усиления в гомо- и гетерохиральных реагентах.
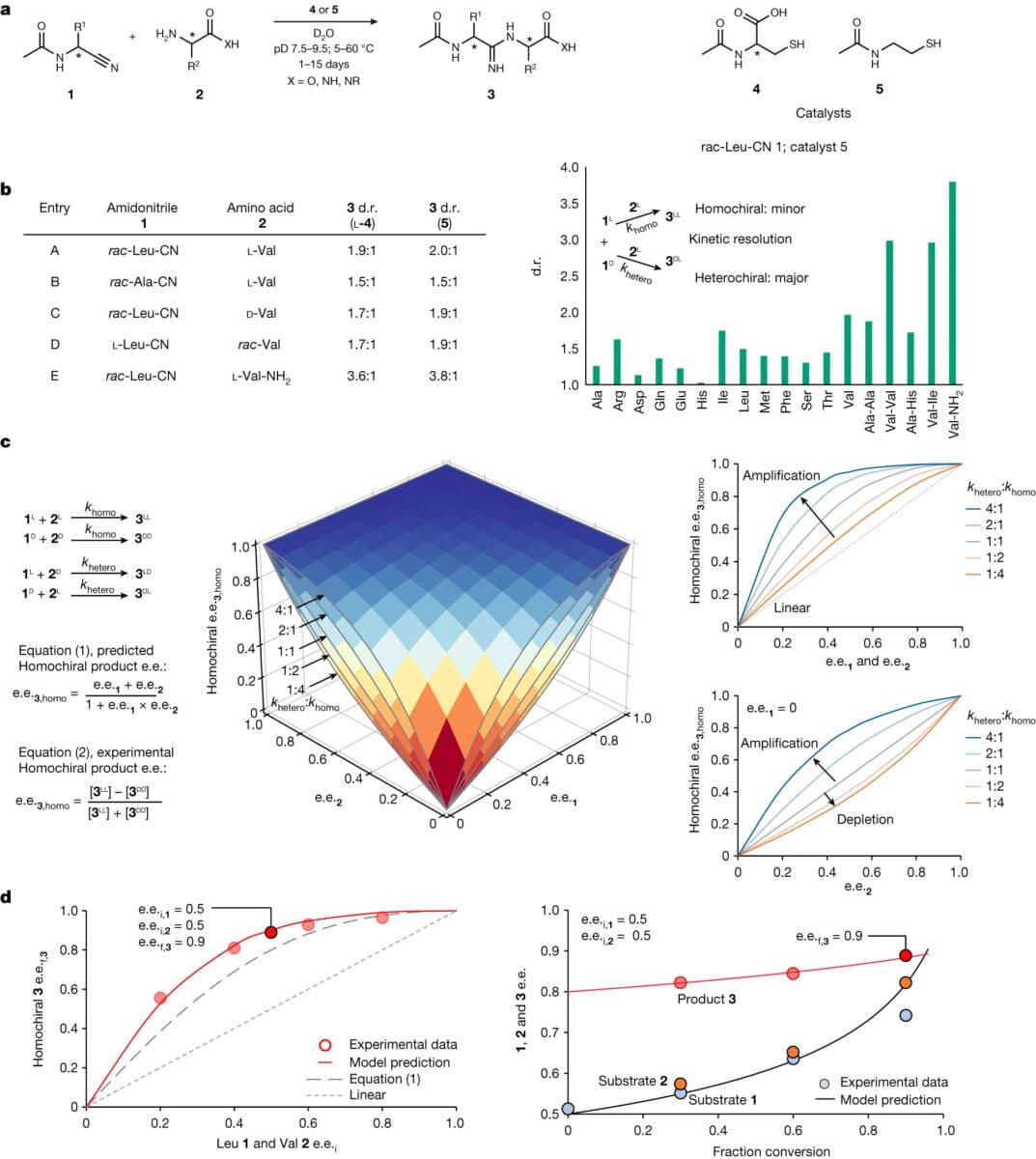
Сначала исследователи создали дипептидный продуктС помощью добавления в раствор соединены две различные аминокислоты. тиолаАвторы не открыли эту реакцию, но первыми исследовали её с позиции формирования гомохиральности.
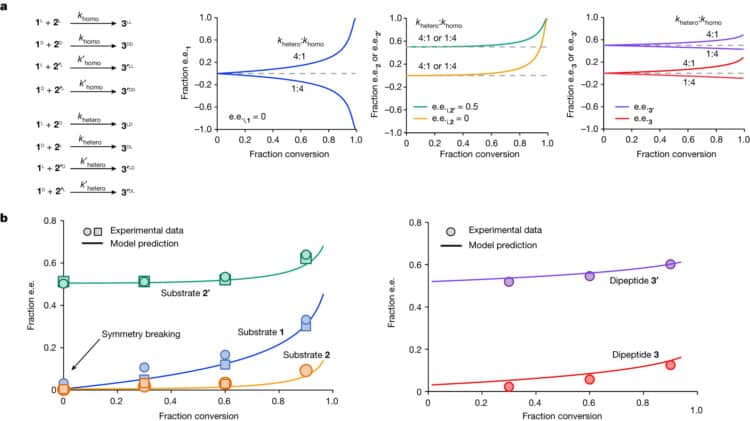
Эксперимент показал: при образовании дипептида в смеси с избытком левых энантиомеров симметрия нарушается, и количество молекул, закрученных налево, больше.
Если в исходной смеси левосторонних аминокислот больше, чем правосторонних, то быстрая реакция соединения лево- и правосторонних аминокислот быстро исчерпает правосторонние. Это увеличивает концентрацию левосторонних молекул.
Гетерохиральные пептиды склеивались и осаждались, оставляя в смеси только гомохиральные L-аминокислоты. Авторы отмечают, что добавление ахирального катализатора (например, молекул тиола) привело к такой же селективности пептидов в реакции, как и левосторонний катализатор. Исследователи считают этот факт свидетельством большей вероятности возникновения гомохиральности в пребиотических условиях с помощью подобной системы.